Ejemplos de bases, Hidróxido de Potasio KOH, Hidróxido de Aluminio Al(OH)3, Amoniaco NH3, Hidróxido de Amonio, NH4(OH), Hidróxido de Calcio Ca(OH)2, Hidróxido de Litio LiOH, Amiduro de Sodio NaNH2, Hidruro de Sodio HNa, etc.
El científico sueco Arrehenius que inicio con la física y posteriormente se intereso en la química. Explica que las bases corresponden a todas aquellas sustancias que pueden liberar iones OH- , cuando entran en contacto con el agua. Más tarde los cientificos Brönsted y Lowry establecieron la siguiente definición para base:
” Base: Es la sustancia alcalina que puede o tiene las propiedades idoneas para incluir en su composición un proton H+ “.
Por lo que la química moderna toma como valida la definición hecha por Brönsted y Lowry, al ser más completa.
Debido a que la base es medida por su nivel de alcalinidad, si su pH es de casi 7 se considera baja, pero si es de 14 su pH es considerada alta, entonces recibe el nombre de superbase.
Ejemplos de bases:
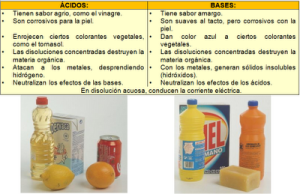
- Hidróxido de Sodio NaOH
- Hidróxido de Potasio KOH
- Hidróxido de Aluminio Al(OH)3
- Amoniaco NH3
- Hidróxido de Amonio NH4(OH)
- Hidróxido de Calcio Ca(OH)2
- Hidróxido de Litio LiOH
- Amiduro de Sodio NaNH2
- Hidruro de Sodio HNa
- Hidróxido de Cromo Cr(OH3)
Ejemplos de bases debiles:
- amoníaco, NH3
- metilamina, CH3-NH2 (todas las aminas en realidad)
- piridina, C5H5N
- hidróxido de amonio, NH4OH
- hidracina, NH2-NH2
Ejemplos de bases fuertes:
- NaOH hidroxido de sodio
- LiOH hidroxido de litio
- KOH hidroxido de potasio
Clasificación de bases:
Bases de Bronsted: porque son aquellos compuestos que son capaces de captar un protón. ejemplos de bases: OH-
Bases de Lewis: se debe a que los compuestos con pares de electrones pero sin compartir, si pueden atraer a un par de electrones para formar un enlace. Ejemplos de bases es el NH3
También existe una interacción entre los ácidos y las bases, logrando clasificarse en dos tipos:
-
Fuertes
-
Débiles
- Los fuertes, se debe a que existe una solución que se puede dosociar como es el caso de NaOH.
- Débiles, por la solución se puede ionizar solo una parte como es el caso de NH3.
En el caso de las bases fuestes como es con KOH, se logra una disociación total, como se muestra en el siguiente ejercicio:
KOH -> K+ + HO-
Cuando es en el caso de los débiles, entonces se replantea el equilibro que se mantiene en una constante de su basicidad, como lo demuestra el siguiente ejercicio:
NH3 + H2O <-> NH4 + + HO-
Kb = [NH4 +].[HO-] / [NH3]
Destacandose asi las bases fuertes en los ejemplos de bases:
Fuerte:
- NaOH, hidróxido de sodio.
- KOH, hidróxido de potasio.
- Ca(OH)2, hidróxido de calcio.
- CsOH, hidróxido de cesio.
Débil:
- NH3, amoníaco .
- CH3-NH2, metil amina.
- NH4OH, hidróxido de amonio.
- piridina.
- Al(OH)3, hidróxido de aluminio.
- Fe(OH)3, hidróxido de hierro (III).
Para que comprendas en que consisten las bases te explico lo siguiente:
Todos los seres vivo estamos compuestos por proteínas, que al recibir ácido, ocasiona que la estructura se alteren así como sus funciones. Por tal motivo, las enzimas se empiezan a lesionar y actuar de forma caótica.
En relación a las bases fuertes, es menos potente su efecto, pero si ocasiona daño, por ejemplo la sosa caustica, primero vulnera la piel quemando y provocando que se ponga una especie de capa jabonosa por el efecto de la grasa corporal. Sin embargo si puede letal en caso que entre en contacto con la vista, debido a que es más sensible y puede ocasionar ceguera total.
[…] Ejemplos de Bases […]