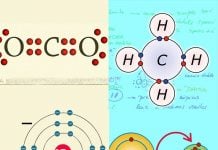
Ejemplos de moléculas, se define como la más pequeña de las partículas de una sustancia, que existe en estado libre y que conserva sus propiedades.
Todas las de una misma sustancia son semejantes entre sí.
Ejemplos de moléculas de sustancias
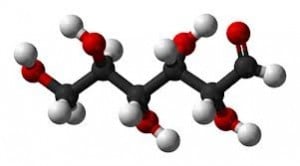
Una sustancia compuesta o simple es una yuxtaposición de un gran número de moléculas.
Un litro de agua es conformado por la unión de de miles de millones de moléculas de agua semejantes entre sí. Cada una de ellas mantiene las propiedades del agua.
De rayos X:
Al analizar los rayos X de los átomos de yodo nos encontramos con los átomos agrupados en pares, entonces se trata de molécula biatómica.
Dentro de este caso es similar el nitrógeno, el hidrógeno, el oxígeno y el cloro entre otros.
De Vapor de fósforo:
El vapor de fósforo se forma por moléculas de cuatro átomos, entonces se trata de moléculas tetratómicas.
Del mercurio:
Como Ejemplos de moléculas del mercurio y otros metales se constituye el vapor por átomos separados, dando lugar a moléculas monoatómicas.
Molécula:
Un ejemplo claro de la vida cotidiana:
Coloca en un vaso de agua solo unos granos de azúcar y déjalo estacionar por un tiempo.
Luego de ese tiempo habrán desaparecido los granos porque se disolvió el azúcar.
Los granos de azúcar se dividieron en pequeña partes: en moléculas.
Cada una de las moléculas de agua pueden ser divididas en más pequeñas partes, en este caso se llaman átomos, con lo cual no obtienes agua.
Las discretas:
Como Ejemplos de moléculas discretas son las que se forman con una cantidad determinada y fija de átomos con distinto o igual elemento, polímeros o macromoléculas. Es decir que se forman por gran cantidad de átomos.
Polímeros o macromoléculas:
Se constituyen por la sucesión de una unidad simple o conjunto que se encuentra limitado por esas unidades y llegan a tener un peso molecular de relativo alcance alto.
Modelos o fórmulas moleculares:
A partir de un modelo o fórmula molecular se describe las moléculas y los compuestos.
Los químicos las utilizan para describir y escribir sobre las moléculas indicando su comportamiento en las reacciones químicas.
Es una notación especial, la cual indica los elementos que constituyen la molécula y la cantidad de átomos que necesita cada elemento.
Por ejemplo:
ADN
Hidróxido de Litio LiOH
Monóxido de Carbono CO
Bióxido de Carbono CO2
Metano CH4
Ácido clorhídrico HCl
Cloro Cl2
Oxígeno O2
Hidrogeno H2
Agua H2O
Cómo se forman:
Los átomos que la forman compartiendo enlaces entre sí se llama enlace covalente.
Son iguales en las sustancias simples y diferentes en las sustancias compuestas.
No obstante tienden a mantenerse aisladas o a veces unidas debido a débiles fuerzas entre sí con características como:
En la temperratra ambiente son generalmente gases.
En menos casos líquidas como por ejemplo el agua o sólidas como en el caso del yodo.
No son conductoras de energía eléctrica.
Cuentan con bajos los puntos de ebullición y fusión.
Las covalentes sólidas se caracterizan por un aspecto céreo, blando y quebradizo.
Si quieres saber sobre sustancias, lee: ejemplos de sustancias puras.